心不全に対して行う治療にはどんなものがあるか:薬物以外の治療(心臓カテーテル治療、手術、ペースメーカー、緩和ケアなど)
心不全の治療法は多岐にわたります。心不全に対する治療では原因に即した治療法が選択されます。このページでは薬物以外の治療(
目次
1. 心臓カテーテル治療
医療行為に用いられる細い管のことをカテーテルと言います。これを血管や尿道、腹腔などに挿入して行う治療をカテーテル治療と言います。心臓の治療でもカテーテル治療が行われます。
心臓と血管はつながっています。血管に入れたカテーテルを心臓に到達させて行う心臓の治療を
冠動脈形成術(PTCA、PCI)
心臓カテーテル検査と同じ要領で、手首の動脈(
カテーテルやワイヤーを用いて冠動脈の細くなっている部分を内側から風船を使って拡げます。この際に
- BMS(Bare Metal Stent:薬剤のついていないステント)
- DES(Drug Eluting Stent:薬物溶出性ステント)
元来BMSしかなかったのですが、ステントを留置したのに血管が狭くなる現象(再狭窄)が見られたためDESが開発されました。DESは薬剤溶出性ステントという名前の通り薬が塗ってあるステントです。
血管
【DES(薬剤溶出性ステント)の特徴】
| DES(薬剤のついているステント) | |
| 長所 |
|
| 短所 |
|
不整脈の治療:カテーテルアブレーション
心臓は血液を全身に送り出すために定期的に拍動しています。そのために洞結節という部位が定期的な電気信号を発信しています。洞結節からの電気信号を受けて動くために心臓には電気回路があります。
【心臓の電気伝導系の略図】

この回路が正常に機能していない場合や別の電気回路がある場合、洞結節以外から電気信号が来る場合に不整脈が起こります。
カテーテルアブレーションの方法のあらましを説明します。心臓カテーテル検査と同じ要領で血管にカテーテルを入れて心臓に到達させます。到達したカテーテルの先から高周波の電流を流すことができます。この強い電流によってカテーテル先端周囲の心臓組織が焼かれて細胞は壊死します。「異常な電気信号を出す部位やその周辺」や「別の電気回路のある箇所」の細胞が壊死すれば、不整脈は出現しなくなります。
カテーテルアブレーションですべての不整脈を治療できるわけではありません。治療できる不整脈の主なものは以下になります。
症状や
一方で、正常な部位を焼いてしまうと正しい電気回路が保てなくなるため、焼く前には慎重な確認作業が必要です。
- 治療前の
心電図 から問題となっている部位や問題となっている現象を推定する - カテーテルアブレーションを開始する前に、心臓に入れたカテーテルを用いて電気生理学的検査(EPS : Electrophysiological study)を行い、異常な部位を詳細に確認する
正しい電気回路が維持できなくなると
カテーテルアブレーションの最も優れた点は、治療がうまくいった場合に根治できることです。薬物療法を行っても根治は難しく、長期的に薬を飲まなくてはなりません。
カテーテルアブレーションは優れた点を持つ治療ですが、
弁膜症の治療:TAVI、マイトラクリップ
心臓には血液逆流防止弁が4つあります。それらのうち
【心臓の図】

大動脈弁が狭くなると心臓から全身に血液を送り出すのが難しくなります。これを大動脈弁狭窄症といいます。以前は大動脈弁狭窄症の治療に選択肢が少なく、手術で弁を取り替える方法(大動脈弁置換術)か薬で治療する他ありませんでした。
心臓の手術は身体にとても大きな負担が強いられます。そのため、心不全などで体力の落ちている人や高齢者は薬物治療を選択することが多かったのですが、薬物治療は症状を和らげる効果はあっても弁膜症を根治できないことが問題でした。そこで、カテーテルを用いて大動脈弁狭窄症を治療できないかと開発されたのがTAVI(Transcatheter Aortic Valve Implantation:経カテーテル大動脈弁留置術)です。
この治療法では、足の付け根の動脈(大腿動脈)や鎖骨の下の裏の動脈(鎖骨下動脈)からカテーテルを挿入したり、心臓の前側の先端(心尖部)から直接カテーテルを挿入したりして大動脈弁の治療を行います。
カテーテルを大動脈弁の位置まで到達させると、そこで風船を拡げて狭くなっている弁を押し広げます。同時に、風船を拡げたタイミングで新たな生体弁をそこに留置することで、大動脈弁の効力を回復させます。
この治療は胸を大きく開いて手術する必要が無いので、患者さんの身体への負担が少ないことが特徴です。特に生活の質(
今まで弁膜症の治療にカテーテルが用いられるのは大動脈弁狭窄症のみでしたが、2017年11月に国内で僧帽弁閉鎖不全症にもカテーテル治療が行えるようになりました。
この治療はTAVIと同じくカテーテル治療ですので、身体への負担が軽いことが特徴です。一方で、手術による僧帽弁置換術も有効な治療法ですので、どちらが患者さんに適しているのかについて症状や年齢から慎重に検討されます。
心房中隔欠損症の治療
心臓には左右と上下に4つの部屋(左心房、左心室、
【心臓の図】

4つの部屋のうち左心房と左心室の間の壁に穴が開いている状態を心房中隔欠損症といいます。穴が小さく症状もない軽症であれば特に治療を行わないで良い場合もありますが、穴が大きく症状が出ている場合には心不全や不整脈の出現が懸念されるため治療が検討されます。
治療法には手術とカテーテル治療があります。カテーテルを用いた閉鎖栓(アンプラッツァーやオクルテックなど)治療を行えば身体の負担が軽く済むため退院が早くなるメリットがありますが、開いている穴が大きいとカテーテル治療では塞ぎきれません。そのため症状や穴の大きさなどから治療法が選択されます。
2. 外科的治療(手術)
心不全の原因が心臓や冠動脈(心臓に栄養を含んだ血液を送る血管)にあるとき、心臓の手術を行うことで心不全を改善させることがあります。
この章では心臓手術はどういう人にどうやって行われているのかについて説明します。
冠動脈疾患:冠動脈バイパス術(CABG:Coronary Artery Bypass Grafting)
心臓に栄養を送る動脈のことを冠動脈といいます。冠動脈は右側に1本(右冠動脈)と左側に2本(左前下行枝、左回旋枝)あり、心臓を取り巻くように存在します。

この冠動脈が細くなると、心臓は栄養が少ない中で動かなくてはならなくなります。冠動脈は多少細くなったくらいではあまり自覚症状は出てきませんが、非常に細くなると段々と症状が出てきます。最初は動いたときに胸痛や息切れを感じるようになり、さらに進行すると動かなくても胸痛や息切れが現れます。大別すると、前者を狭心症と言い後者を心筋梗塞と言います。
近年の医療技術の進歩によって、狭心症や心筋梗塞は開胸手術を行わなくても治療することができるようになりました。血管を介して治療を行うカテーテル治療は身体への負担が手術よりもだいぶ軽く済むため、狭心症や心筋梗塞の治療における主流になりつつあります。
しかし、冠動脈バイパス術は廃れることのない有効な治療です。というのも、左冠動脈主幹部(左前下行枝と左回旋枝に分かれる前の根元の動脈)が狭い場合や3本の冠動脈の全てが狭い場合にはカテーテル治療を受けることができない可能性が高いです。そのため狭くなった冠動脈を助ける血管を作る手術(バイパス術)が必要になります。
冠動脈が狭くなるとその下流には血液が行き渡りにくくなります。冠動脈バイパス術では、血液の足りなくなっている下流に対して新しい血管(バイパス)を作って血液を補充します。このバイパスに主に用いられる血管は内胸動脈・大伏在静脈などです。
カテーテル治療に比べて身体の負担が大きく傷跡も残りますが、確実に血流を確保できることが利点になります。またカテーテル治療は留置したステントが詰まったり、治療後に抗血小板薬(血をサラサラにする薬)を飲まなければならなかったりするため、患者さんの状況によって治療法が選択されます。
心臓弁膜症:弁置換術、弁形成術
心臓には血液の逆流を防止するための弁が4つあります。それらのうち左心室と大動脈の境目にある逆流防止弁を大動脈弁といいます。
【心臓の図】
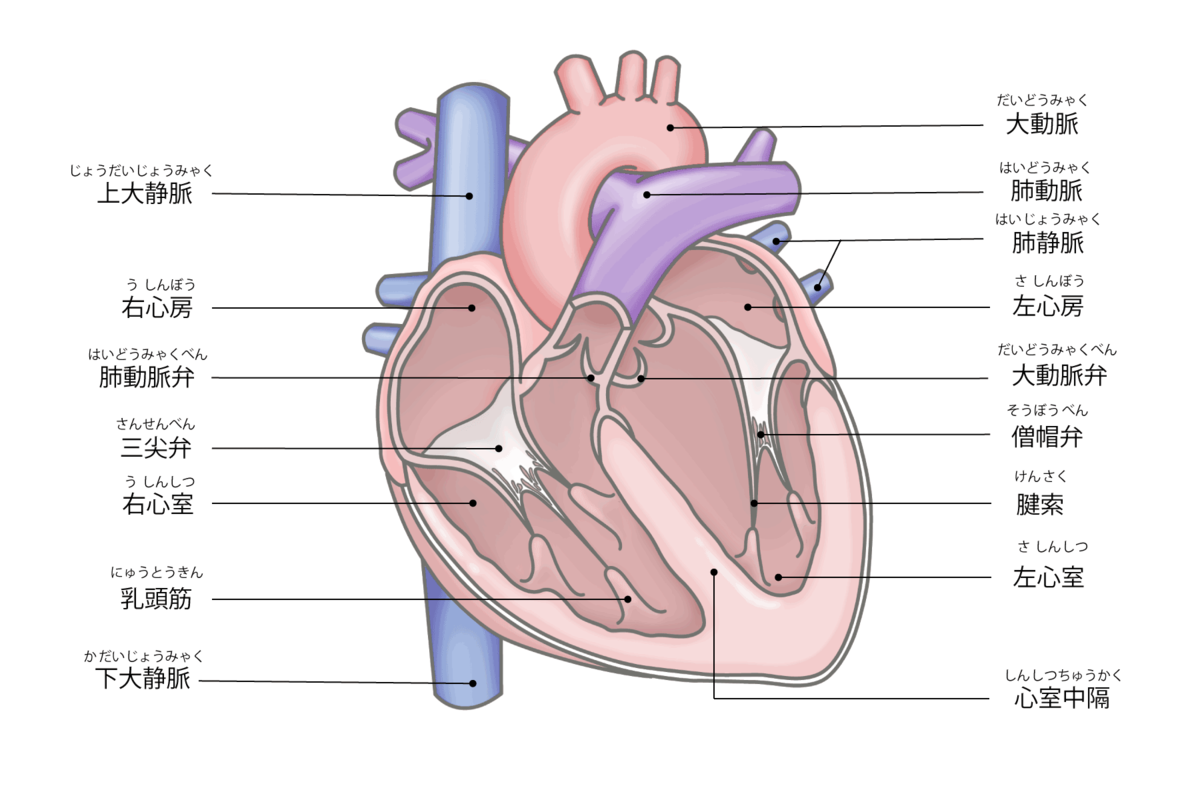
逆流防止弁がうまく機能しなくなると、血液が逆流したり(閉鎖不全症)、血液を送り出しにくくなったり(狭窄症)します。この状態を弁膜症といいます。弁膜症の程度が悪化し症状が出るようになると、手術で弁の機能を回復することが検討されます。弁の機能を回復させる手術は以下の2つです。
- 弁置換術
- 弁形成術
「弁置換術」は機能の低下した弁を取り除いて新たな弁と取り替える手術です。その際に用いられる弁には生体弁と機械弁の2つがあります。この2つにはメリットとデメリットがあるためどちらを用いるかは、患者さんの背景を踏まえて考える必要があります。
【生体弁と機械弁の違い】
| 生体弁 | 機械弁 | |
| 素材 |
|
|
| 耐久性 |
|
|
| 血栓のできやすさ |
|
|
| 感染 |
|
|
年齢から推測される平均寿命までに行う必要のある再手術の回数や内服継続かどうかなどの環境などの多くのことを考えて判断します。
一方で、「弁形成術」は患者さんの弁を活かして、周囲の環境を整えることで弁の機能を回復させる手術です。弁置換術よりも血栓症や感染症が起こりにくいとされています。しかし一方で、全ての弁膜症に対して弁形成術が行えるわけではありません。特に大動脈弁の弁膜症では弁形成術を行うことが難しいため、弁置換術が行われることが多いです。他の弁の弁膜症では基本的に弁形成術が行われますが、弁形成術が行えない状況では弁置換術が行われます。弁形成術でも手術後に数ヶ月は抗凝固薬を飲む必要があります。
心房中隔欠損症
右心房と左心房の間の壁(中隔)に穴が開いている病気を心房中隔欠損症といいます。症状がない場合には特に治療を必要としませんが、症状が出てきた場合には心不全のときに用いる治療薬を使用します。
病状がさらに進行するとカテーテル治療や手術によって開いている穴を閉じる必要が出てきます。カテーテル治療は身体への負担が少ないため行う場面が多いですが、カテーテル治療が行えない場合には手術を行います。
手術では胸を開けてから心臓を切開して、右心房と左心房の間にある壁の穴を確認します。穴の大きさや位置を確認して、あてもの(パッチ)を充填して穴を埋めるか、
心室中隔欠損症
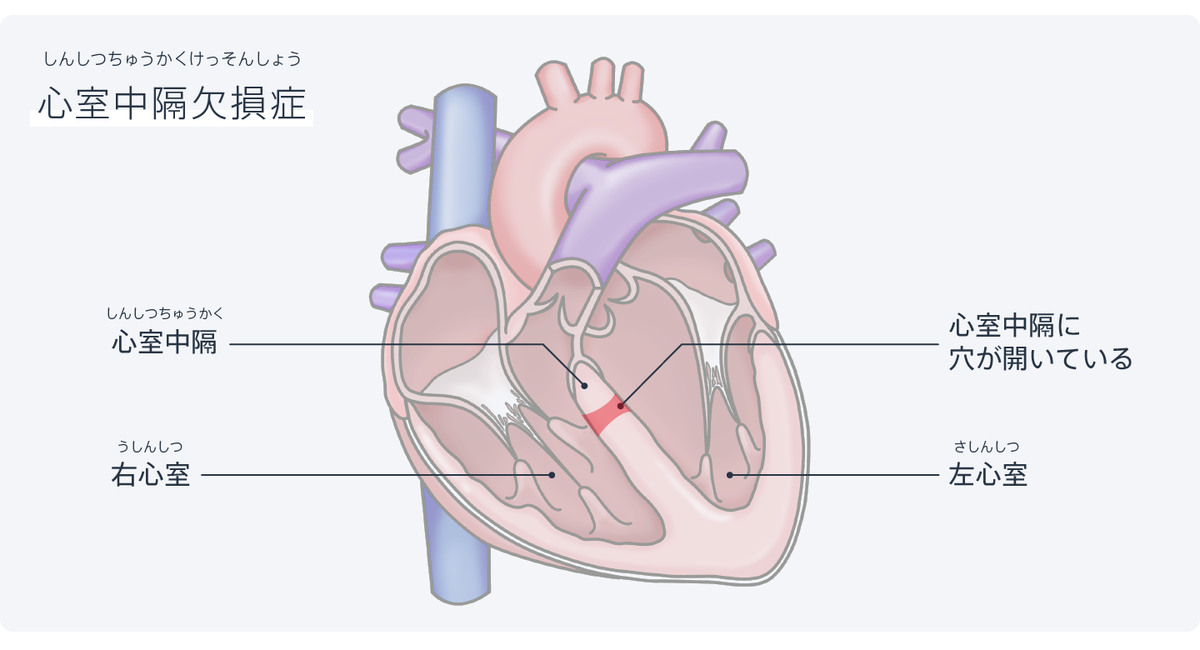
心室中隔欠損症は右心室と左心室の間(心室中隔)に穴が開いている病気です。心室中隔欠損症は比較的多い病気で、こどもの先天性心疾患(生まれつきの心臓の病気)の20%ほどと言われています。この病気があると左心室から全身に送られるべき血液の一部が右心室に流れてしまうので、効率的に全身に血液を送れなくなってしまいます。
治療法は開いている穴の大きさや位置によって異なります。開いている穴が小さくて特に症状がない場合には、そのうち穴が自然と塞がることがあるので治療を行わずに様子を見ます。一方で、穴が大きくて症状(息が切れる、
胸を切開してから心臓を開いてから、あてもの(パッチ)を用いて穴を閉じます。手術後はだんだんと状態が改善し、周囲の子供と同程度に発育するようになります。
不整脈:メイズ(MAZE)法
心房で起こった異常な電気信号が不規則に心臓に伝わることで心房細動という不整脈が起こります。心房細動を治療するのに手術を行うことがあります。
心房で起こった異常な電気信号が心室に伝わらないように、手術で異常な電気回路を遮断します。開胸したのちに、問題となっている部位に対して高周波装置を用いて心筋を壊死させることで電気回路を遮断します。
この手術をメイズ法といいますが、どんな人にも行うことのできる手術ではありません。メイズ法が適していると考えられるのは次のような人です。
- 僧帽弁の弁膜症に
合併 した心房細動がある人に弁形成術あるいは弁置換術を行う場合 - 弁膜症や心房中隔欠損、冠動脈疾患などの心臓病に伴う心房細動に対して手術を行う場合
- 適切な治療(抗凝固療法、血栓溶解療法)を行っているにもかかわらず左房内に血栓が存在する場合やその左房内血栓が
塞栓 症を起こしたことがある場合 - カテーテルアブレーションがうまくいかない場合や再発する場合
不整脈や心不全の状況を鑑みて手術の適否が決まります。心房細動には手術以外にも多くの治療法が存在しますので、心房細動に悩んでいる人は主治医とよく相談して納得した治療法を選ぶようにして下さい。
収縮性心膜炎
心臓の周囲は膜(壁側心膜と臓側心膜)が覆っています。この心膜に
収縮性心膜炎が原因で心不全に至った人には手術が行われます。固まってしまった心膜を切除したり剥がしたりすることで、心臓を動きやすくします。症状が高度に進行してから手術を行ってもあまり改善が見られない状況が多いことが分かっているので、手術を行う場合には適切なタイミングを判断する必要があります。
拡張型心筋症:バチスタ手術
心臓は筋肉の塊のようなもので、その中に血液が入る部屋が4つ存在しています。拡張型心筋症は心臓が大きくなっていくことで筋肉がだんだんと伸びていく病気です。ちょうど伸びたゴムのように心臓の筋肉も弾力性を失ってしまうため、拡張型心筋症になるとうまく血液を全身に送り出せなくなり、心不全になりやすくなります。
心臓を移植することも治療の一つですが、バチスタ手術も拡張型心筋症に有効と考えられています。バチスタ手術は1996年にバチスタ医師が発表しました。拡張して弾力性を失った心臓の筋肉の一部(側壁)を切り取って残った部分を縫い合わせることで、心臓を小さくする手術です。この手術で心臓は弾力性を取り戻すことができます。
現段階ではバチスタ手術はすべての人に対して適しているわけではありません。また、この手術を行える医療施設は限られています。拡張型心筋症に困っている人は偏った情報だけで判断を急がずに、自分にはどの手術が適しているのかについて主治医とよく相談するようにして下さい。
身体の負担を最小化する手術:MICS(Minimally Invasive Cardiac Surgery)
元来の心臓手術は胸骨を縦に20-30cmほど切開して行っていたため、身体の負担が大きく、手術後のリハビリテーションが難しい状況でした。近年、より体に負担をかけないために、小さな切開で手術を行おうという試みがなされています。この手術を低侵襲性心臓弁膜症手術(M
肋骨の間や胸骨を10cm弱ほど切開して手術を行うので、通常よりも半分以下の傷口で済みます。そのため、身体への影響は小さくすることができますし、見た目も傷跡が目立ちにくくなります。
全ての心臓手術でMICSが行えるわけではありません。MICSについて知りたい方や希望のある方は、手術を行う医師に尋ねてみてください。
3. 酸素療法
肺は生命の維持に必要な呼吸を司る臓器です。大きく次の2つのことを行っています。
- 体外から血液中に酸素を取り込む
- 血液中から体外に二酸化炭素を取り出す
心不全で肺の血液がうっ滞すると、肺や
急性心不全の
- SaO2(
動脈血 液の酸素飽和度)が95%以上 - PaO2(動脈血液の酸素分圧)が80mmHg以上
これを下回るときには酸素療法を行います。鼻カニュラ(細い管で左右の鼻にあてる位置に2つの穴がある)あるいは酸素マスクを用いて酸素を投与します。
もともと肺に病気(COPD、気管支喘息、間質性肺炎、肺結核後遺症など)がある場合には酸素療法は注意が必要です。その背景には呼吸を司る体内における酸素や二酸化炭素濃度ののセンサーが鈍っていることがあります。
- 酸素を多く体内に取り込むと体内で作られる二酸化炭素が増える
- 肺の持病が重い人は二酸化炭素が増えるとうまく体外に出せない
- 体内に二酸化炭素が貯留する
- 体内に二酸化炭素が溜まると呼吸が増えるが、もともと肺に持病があると二酸化炭素が溜まっても慣れているため呼吸が増えない
- 酸素を投与しているので体内の酸素は足りているため、呼吸を減らす方向に身体が反応する
つまり、酸素が足りていないから酸素を投与したのに、かえって呼吸数が減って状態が悪化してしまうのです。このパラドックスを
そのため、酸素療法を開始して二酸化炭素が溜まってしまう人などでは酸素療法は適していません。
- PaCO2(動脈血液中の二酸化炭素分圧)が50mmHg以上(通常は40mmHg)
- 酸素投与をしても息苦しさが改善しない
- 酸素投与をしても呼吸が荒い
- 酸素投与をしても座らないと呼吸ができない
これらに当てはまる人は人工呼吸器管理を開始します。人工呼吸管理については次の段落で詳しく説明します。
4. 人工呼吸器管理
人工呼吸器は自力で十分な呼吸ができない人に対して呼吸のサポートを行います。体外から強制的に呼吸をさせたり、自発的な呼吸を楽にするように圧力をかけたりできます。
人工呼吸器は大きく分けると次の2つです。
- 気管挿管を行わない人工呼吸器管理
- 気管挿管による人工呼吸器管理
ここで気管挿管という聞きなれない言葉が出ています。気管挿管とは口から管を入れることを指します。管は親指程度の太さで、口から気管に到達します。この管を通して直接肺につながるパイプを設けた上で、人工呼吸器が呼吸をサポートします。
この2つの人工呼吸器管理の特徴について次の段落で説明します。
気管挿管を行わない人工呼吸器管理:NIPPV(非侵襲性陽圧換気)
気管挿管を行わない人工呼吸器管理は身体の負担が比較的軽いことから非侵襲性陽圧換気(NIPPV:Non-Invasive Positive Pressure Ventilation)と呼ばれています。NIPPVでは、顔に密着するマスクを用いて呼吸をサポートします。バンドを使ってほとんど漏れる部位がないくらい密着させます。
【NIPPVのマスク】

マスクは人工呼吸器とつながっているため、機械が空気を押し込んだり、息を吐くときに少し圧力をかけて(陽圧をかけて)肺を常に開いたまま呼吸するようにできます。また、人工呼吸器は酸素を多めに体内に送り込むことができます。
強制的に呼吸を促すことができるので、上で述べたようなCO2ナルコーシスによる呼吸の抑制を回避することができます。また、自宅で人工呼吸器管理を行うことができるのも特徴です。
NIPPVの最大の弱点は、マスクがずれたら呼吸をサポートできなくなってしまうことです。そのため、病状が悪くて確実に呼吸のサポートが必要な人にはあまり向いていません。
気管挿管による人工呼吸器管理
心不全の状態が非常に悪い人には確実な呼吸サポートが必要なため、気管挿管を用いた人工呼吸器管理が望まれます。
気管挿管を行うとずっと喉に管が入った状態になるので強い苦しさを感じます。そのため鎮静剤という眠り薬を点滴して痛みや苦しさを感じなくさせる処置が行われます。心臓の状態が改善して、人工呼吸器管理が必要なくなるまでこの処置は行われます。
気管挿管は本来あまり丈夫に作られていない気管に管を通す処置です。長期的に気管挿管を行うと、気管粘膜がえぐれてしまう(
気管切開とは喉の前面に窓のような穴を作ってそこから挿管チューブを入れます。この処置を行うと、気管に潰瘍ができにくくなりますし挿管チューブの取り外しが簡単にできるようになります。
一方で、喉に穴が開くという見た目の問題が残ります。気管挿管が必要ない状態になれば穴を閉じることはできますが、どうしても傷跡は残ってしまいます。
5. 大動脈内バルーンパンピング
大動脈内バルーンパンピング(IABP: Intra Aortic Balloon Pumping)とは心臓の動きを助ける治療です。大動脈内に挿入した縦長の風船が心臓の動きに合わせて膨らんだりしぼんだりします。
心臓の拡張期には風船が膨らみます。膨らんだ風船が圧力をかけることで、心臓のすぐ側にある冠動脈(心臓に栄養や酸素を送る動脈)への血流を増やします。こうして心臓の栄養と酸素を確保するのを効率的にサポートします。
心臓の収縮期には風船がしぼみます。膨らんでいた風船がしぼむことで血管内に陰圧がかかって、心臓から血液が出ていきやすくなります。すなわち収縮期に全身に血液が送られやすくなる仕組みです。
大動脈内バルーンパンピングは、心原性ショックや急性心筋梗塞、不安定狭心症などに対して行われます。血管内に機械を留置するため合併症(血管損傷、動脈解離、血栓症、感染症など)が起こることがあります。そのため、状況を鑑みて必要性とリスクの両サイドから治療するべきが判断されます。
6. 補助人工心臓
補助人工心臓(VAD:Ventricular Assist Device)とは心臓の働きを助ける装置を心臓の外に作る装置です。右心室の働きが弱い人には、右心房から血を抜いて
この装置は年単位の長期間使用することができますので、心不全で長期的にサポートが必要な人に使用可能です。体内に埋め込むタイプと体外に作るタイプの2種類があります。
感染症や出血、血栓症などの合併症が起こるので、生活の中で常に注意が必要です。また、チューブの扱い方も慎重を期す必要があります。
7. 経皮的心肺補助
経皮的心肺補助(PCPS:Percutaneous Cardiopulmonary Support)は人工的な肺を体外に作る
この装置を用いると心臓と肺が連動して行う仕事(右心系の仕事)が楽になるので、心筋梗塞や心不全の超緊急時や心停止の際、重症の
8. 心臓ペースメーカー
ペースメーカーとは不整脈のある人の胸の皮膚の下などに埋め込む機械のことです。心臓がうまく動いていないときに、必要な電気信号を心臓に送ることができます。
皮下に埋め込んである本体から鎖骨下静脈を介して電気信号を伝えるリード(導線)を心臓に到達させます。このリードは2つの役割を担っています。
- 心臓が作る電気信号を感知する(センシング)
- 心臓が動くために必要な電気信号を送る(ペーシング)
不整脈にはペースメーカーで治療できるものと治療できないものがあります。ペースメーカーが有効な不整脈は主に以下になります。
- 洞不全症候群
- 房室伝導障害
不整脈の種類や状態によってセンシングとペーシングに適切なやり方が異なりますので、挿入するペースメーカーも変わってきます。主なペースメーカーのモードは次のものになります。
- AAI
- 右心房の電気刺激を感知して、この刺激を邪魔しないように右心房に電気刺激を送るモードです。
- VVIペースメーカー
- 右心室の電気刺激を感知して、この刺激を邪魔しないように右心室に電気刺激を送るモードです。
- VDDペースメーカー
- 右心房と右心室の電気刺激を感知して、右心室に電気刺激を送るモードです。感知した電気刺激に同期することができます。
- DDDペースメーカー
- 右心房と右心室の電気刺激を感知して、右心房と右心室に電気刺激を送るモードです。感知した電気刺激に同期することができます。
ペースメーカーを用いた治療ではできるだけ心房と心室が協調した動きをするように配慮されます。ペースメーカーにおけるさまざまなモードの中でも、個人の状態を鑑みて最も効率的に動くと予想したモードに設定されます。
CRT:心臓再同期療法
心房と心室が協同した動きをしたときには、心臓の仕事量を無駄なく全身に血液を送る働きに変換することができます。同じように右の心臓(右心房、右心室)と左の心臓(左心房、左心室)が協同して動いたときには無駄のないよい仕事ができます。この考えから行われている治療が心臓再同期療法(CRT:Cardiac Resynchronization Therapy)です。
CRTでは左右の心室をペーシングします。そうすることで心不全の改善が見込まれます。CRTは誰にでも効果のある治療ではありません。効果が期待できるのは次のすべてを満たす人です。
- 心不全治療薬を用いても、軽く動いたただけで息切れや呼吸困難などの症状がある
- 心室興奮時間が0.13秒以上である
- 左心室の駆出率(EF)が35%以下である
CRTも通常のペースメーカーと同じく、前胸部の皮下に本体を埋め込んでリードを到達させます。リードを2本用いて、左右の心室に電気信号を送ります。
ペースメーカーの注意点
ペースメーカーには気をつけなければならない注意点があります。
- 電池寿命がある
MRI 検査を受けられない
この2つは絶対におさえておかなければならないものです。
電池寿命に関しては、定期的な専門外来で残りの電池量を確認して電池切れが起こらないように気をつける必要があります。最近動悸や脈の乱れを感じることが多くなったというような自覚症状がある場合には、必ず主治医に相談するようにして下さい。
また、MRI検査に関しては、強い磁気を浴びるとペースメーカーが停止してしまうことがあるため注意が必要です。しかし、最近のペースメーカーではMRI検査を受けても停止しないものが出てきているため、自分の使用しているペースメーカーはMRI検査に対応できるものなのかどうか一度確認すると良いでしょう。
9. 電気的除細動
心臓の正常な活動では、洞結節(右心房と上大静脈のつなぎ目のあたり)という部位から発せられた電気信号が、房室結節からヒス束を介して左右の心筋に伝わります。
【心臓の電気刺激の伝わり方】

この電気刺激の伝わる回路のどこかに異常がある場合に不整脈が起こります。不整脈は治療薬を用いることでコントロールできる場合が多いですが、重症になるとコントロールが難しく命に関わる状態になることがあります。命に関わるような重症な不整脈に対して電気的
心臓に大きな電流を加えると心筋は脱分極という状態になると考えられています。この状態は不応期といって、他に電気刺激を受けてもこのタイミングの心筋は反応しません。いわば動きがリセットされるような状態ですので、一定時間を経て不応期が終わったタイミングで最初に受けた電気刺激に反応します。
この原理を用いたものが電気的除細動です。心臓に大きな電流を流して心臓の電気刺激を一旦リセットします。不整脈は心臓に対してバラバラに電気刺激が起こっている状態ですが、これをリセットすることで正常な電気刺激(洞結節から伝わる本来あるべき電気刺激)による心臓の運動に回復することが期待できます。
電気的除細動は致死的な不整脈に対して非常に有効な治療方法です。しかし、全ての不整脈に対して有効ではありません。電気的除細動が有効なのは次の2つです。
これ以外にも、血行動態が不安定な状態(血圧が下がる、意識が悪くなるなど)を伴うタイプの心房細動(AF)や心房粗動(AFL)、発作性上室性頻拍(PSVT)でも電気的除細動が行われることがあります。ただ、この場合には意識があることが多いため、鎮静剤を用いた方が良いかあるいはできるだけ早く除細動したほうが良いかなど、状況に応じて患者さんの負担を軽減する配慮が必要になります。
一方で、救急救命の現場で起こる心停止(心臓が止まること)の原因中でも多くを占める次の2つの不整脈に対して電気的除細動を行っても意味が無い(あるいは状況を悪化させる)ことがわかっています。
この2つの状態であれば心臓マッサージを行ったりエピネフリンを用いたりして、正常の電気刺激の回復による心拍の再開を待つことになります。
カルディオバージョン
先ほど述べた電気的除細動とは厳密には定義が異なるのですが、心臓に電気を通して不整脈を改善する治療にカルディオバージョンがあります。カルディオバージョンは基本的にリズムの一定な不整脈に対して行われます。心臓の動くリズムに合わせて大きな電流を流して心筋の動きをリセットするため、リズムが一定でない不整脈には有効ではありません。
主にこれらの不整脈に対してカルディオバージョンは行われます。また、状況によっては心房細動に対してもカルディオバージョンが行われることがあります。
カルディオバージョンは心臓全体に対して脱分極を起こすことが目的ではありません。問題となっている回路(リエントリーと言います)だけがターゲットになります。そのため、カルディオバージョンに用いられる電気的仕事量(ジュール)は、救急救命で行われる電気的除細動よりも小さいものになります。
AEDについて
不整脈によって突然死することはありますが、その一部は電気的除細動を行えば救うことができます。一方で、致死的不整脈はできるだけ早く電気的除細動を行う必要があります。
そこで、医療従事者以外でも使用できる
AEDは2枚のシートを意識を失った人の胸に貼るだけで、心電図の解析を行ってくれます。また、解析の結果除細動が必要(心室細動、無脈性心室頻拍)と判断された場合には、除細動も行うことができます。
とは言え、一般市民がAEDを使う場合には不安を感じる人もいると思います。そこで、BLS(Basic Life Support)という一次救命処置を学ぶ講座があります。BLS講座は誰でも受けることができるため、いつかくるかもしれない救命の機会のためにBLS講座を受けておくことは大切です。この講座では、AEDの使い方のみならず心臓マッサージ(胸骨圧迫)の適切な行い方も習うことができます。
10. 埋込み型除細動器
無脈性心室頻拍や心室細動といった命に関わる重症な不整脈が一度起こると、根本的な解決がなければ次にまた同じことが起こる可能性は高いです。無脈性心室頻拍や心室細動から救命するためには電気的除細動が必要ですが、
埋込み型除細動器を用いた治療は、無脈性心室頻拍や心室細動を経験した患者さんやそれらが起こる可能性が高いと考えられる人に対して行います。この治療はペースメーカーを埋め込むのと同じ要領で、前胸部の皮下に本体を埋め込んで、血管を介してリードを心臓に留置します。このリードを通して異常な不整脈を感知して、必要時には即座に電流を心筋に通してくれます。
ペースメーカーと同じで、強い電磁波を受ける場所(MRI検査室など)には行くことができません。また、誤作動することもあるため、除細動器を埋め込んでから何らかの不具合を感じる人は主治医と相談するようにして下さい。
11. 心臓リハビリテーション
心不全に対する治療の中でも心臓リハビリテーションは非常に重要です。できるだけ心機能を回復させることや心機能を落とさないことが大きな目標になりますが、これ以外にも効果が期待できるとされています。
心臓リハビリテーションとは
日本心臓リハビリテーション学会によると、心臓リハビリテーションとは「自分の病気のことを知ることから始まり、患者さんごとの運動指導、安全管理、
心臓リハビリテーションを行うと運動耐容能(身体が運動の負担に耐える能力)が改善するため、再入院率の低下や長期生命
心臓リハビリテーションは次のことを目標に行います。
- 早期離床(できるだけ早い段階から身体を動かすようにする)して、必要以上に安静にすることによる弊害(褥瘡、肺塞栓症、身体的および精神的なバランスの悪化など)を予防する
- 迅速かつ安全な退院と社会復帰へのプランを立案し実現する
- 運動耐容能の向上によりQOL(Quality of Life:生活の質)を改善させる
- 包括的な患者教育と疾病管理により心不全の重症化や再入院を予防する
急性の心不全で入院しているときはもとより、状態が落ち着いて退院してからもリハビリテーションを継続することでこれらの目標が達成しやすくなります。そのためには、本人の動機づけと成功体験は重要ですので、心臓リハビリテーションをチームで包括的に行う必要があります。また、生活環境の整備や家族の協力は大切な要素になります。
心臓リハビリテーションではどんなことを行うのか?理学療法や運動療法について
ベッドから離れない生活を送っていると、全身の筋肉が衰えて運動能力も下がってしまうため、ますますベッドから離れられなくなります。寝たきりになると心身の状態が落ちてしまうため、うつ病などの精神疾患になることも少なくありません。そこで心臓リハビリテーションは病気から回復するだけではなく、社会生活に復帰することを目標とします。
心臓は筋肉でできています。心臓の筋肉を鍛えることが大切です。心筋が鍛えられると運動ができる範囲(運動耐容能)が広がります。しかし、その人ができる範囲を超える運動負荷をかけるとかえって心臓の状態が悪くなってしまいます。
まず、「自分ができる範囲」がどの程度なのかを医学的に推し量ることが最初のステップになります。「自分ができる範囲」がわかったところで、その範囲を超えない程度の運動メニューを専門のリハビリの先生に作ってもらいます。
次に、こうして作られたメニューを疲れすぎない範囲でこなします。こなしているうちに段々と強い負荷に耐えられるようになってくるので、やれる範囲の運動を根気よく行うことが大切です。
目安となる簡単な目標としては次のものがあります。
- ベッド上の運動(関節の運動など)
- 座った状態を保つ
- 立った状態を保つ
- 短距離を歩行する
- 長距離を歩行する
- 6分間歩行する
- 自転車こぎをする
- 軽いエアロビックスをする
これらをいきなり駆け上がることを目指すのではなく、段階的に達成することが大切です。そうすることで少しずつ状況が好転します。個人の状況によって目標は異なるので、自分の身体のしんどさやリハビリテーション終了後の目指したい生活について、心臓リハビリテーションを開始する前に医療者とよく相談するようにして下さい。
ただでさえ心不全によって苦しい状態なのに運動するとさらに苦しさを伴います。しかし、運動療法によって得られる効果は大きいので、運動療法はよほど重症(NYHA4度程度)な心不全でない限り行うべきです。自分の治療がどのくらいの効果があるのかを知らないで苦しいことを続けるのは非常に苦痛ですので、患者さん自身が運動療法の効果を知っておくことは大切です。
- 運動耐容能の改善
- 心臓への効果
- 左心室機能:安静時の左室駆出率不変または軽度改善、運動時の心拍出量増加反応の改善、拡張早期の左心室機能改善
- 冠循環:冠動脈内皮機能改善、運動時心筋灌流改善、冠側副血行路増加
- 左心室リモデリングの抑制
- 末梢効果
- 骨格筋:筋量増加、筋力増加、有酸素条件下の代謝改善、抗酸化
酵素 の発現増加 - 呼吸筋の改善
- 血管内皮:内皮依存性血管拡張反応の改善、一酸化窒素合成酵素発現の増加
- 骨格筋:筋量増加、筋力増加、有酸素条件下の代謝改善、抗酸化
- 神経体液因子
自律神経 機能:交感神経 の活性抑制、副交感神経 の活性亢進,心拍変動の改善- 呼吸:呼吸中枢CO2感受性改善による換気応答の改善
- 炎症マーカー:炎症性サイトカイン(TNFα等)低下、
CRP 低下
- QOL(生活の質)の改善
(『慢性心不全治療ガイドライン(2010年改訂版)』を参考に作成)
非常に細かい内容ですので全てを把握する必要はありませんが、心臓リハビリテーションによって心機能・呼吸・神経などに良い効果があることは知っておくと良いでしょう。
精神的サポート
心不全で入院加療を受けるとき、さまざまな不安や恐怖が襲ってきます。突然現れた症状の苦痛や今後のことへの不安、究極的には死への恐怖などさまざまなプレッシャーを感じます。こうした不安や恐怖から一時的な錯乱(せん妄)状態になる人も多いです。また、精神的に落ち込んでしまい、うつ状態になる人も少なくありません。
【心不全のNYHA分類とうつ状態の関連】
| 心臓の重症度(NYHA) | うつ状態の |
| Ⅰ | 11% |
| Ⅱ | 20% |
| Ⅲ | 38% |
| Ⅳ | 42% |
今までできていたことができなくなる不安や羞恥心も大きく、心不全患者に対する精神的なサポートは重要です。一方で、自宅においても精神的なサポートは重要です。リハビリテーションに対するモチベーションを保つのに一役買えるサポートです。
『急性心不全治療ガイドライン(2011年改訂版)』では次のサポートが有効であると述べています。
- 早い時期から家族との面会時間を確保する
- 患者の訴えを遮らずに聞く
- 検査や処置の前にその目的や方法を説明し不安を取り除く
- 不安や疑問を訴えやすいように積極的に声をかける
- 睡眠時間を確保するように配慮する
- 活動制限や面会制限によってストレスが増大しないように気分転換できる活動を考慮する
- 検査や治療、リハビリの計画を説明することで、患者が自分の今後の予定をイメージしやすいようにする
- 落ち着きのなさや不眠が続く場合は
不穏 やCCU症候群を疑い、予防的対処を考える
心臓リハビリテーションに対して必要なサポートは個人個人で異なります。本人やその家族と医療者がよく話し合うことで、最適なサポートを目指します。
参考文献
・日本循環器学会ほか, 急性心不全治療ガイドライン(2011年改訂版)
・日本循環器学会ほか, 慢性心不全治療ガイドライン(2010年改訂版)
・Depression in Heart Failure: A Meta-Analytic Review of Prevalence, Intervention Effects, and Associations With Clinical Outcomes. J Am Coll Cardiol 2006;48(8):1527-37
患者の知識向上のために必要なもの
入院中は医療者が患者さんの状態について細かく管理してくれます。治療はもちろん生活の状況や体調面などさまざまなことを見てくれます。
- 食事
内服薬 - 運動
- 体重
入院中はこれらをチェックしながら心不全の状態が管理されますが、退院した途端に医療者の管理がなくなります。通院や訪問看護などを行いながら定期的に状態が確認されますが、日常で心不全の状態を管理するメインプレーヤーは医療者から自分自身に変わります。そのため患者さん自身が病気を正しく把握して、生活を改善することはとても大事です。
退院後は次のことに気をつけると良いです。
- 毎日の体重測定と目標体重の比較
- 目標体重よりもだんだんと増えていくような場合には心不全の悪化を考える
- 心不全再発時の症状や身体の変化を知っておく
- 症状や身体の様子を毎日自己チェックし悪化の早期発見に務める
- 服薬を遵守し継続する
- お薬カレンダーなど飲み忘れがないための工夫
- 塩分摂取を制限する
- 軽症の心不全:7g以下/日
- 重症の心不全:3g以下/日
- 過度のアルコール摂取を控える
- アルコール性心筋症の場合は完全な断酒が必要
- 禁煙する
- 適度な運動療法を継続する
- 身体への負荷が強すぎても良くない
- 心臓に関わる持病を適切に管理する
患者さんの知識向上は、運動耐容能の改善やQOLの向上のみならず再入院の予防にも重要です。知っておくポイントを医療者にあらかじめ聞いておくようにして下さい。
12. 食事療法
心不全の食事におけるポイントは塩分と水分を摂りすぎないことです。また、どの程度の制限をかけるかは心不全の重症度によって異なります。
簡単な目安は以下になります。
【心不全の重症度ごとの水分と塩分の目標摂取量の目安】
| 1日の目標塩分摂取量 | 1日の目標水分摂取量 | |
| 軽症の心不全 |
|
|
| 重症の心不全 |
|
|
また、肥満がある場合は減量を目標としたカロリー制限をする必要があります。
上の表の数字は目安です。どのくらいのカロリーバランスの食事をするべきかは個人差があるので、主治医や管理栄養士に相談するようにして下さい。
13. 和温療法
和温療法は日本発の薬を用いない心不全の治療方法です。サウナや毛布を用いて身体を温めることで心不全の治療を行います。
温度を高めることで心拍数が増えますが、血管が拡張することによって心臓の前負荷の軽減や肺高血圧の改善が見込まれます。大動脈弁狭窄症や肥大型閉塞性心筋症に対しては適していませんが、それ以外の慢性心不全に対しては効果が期待できます。
一方で、脱水に対する注意深い観察が必要で、発汗量と同程度の水分の摂取を行わなければなりません。また、保険適応ではないことに注意が必要です。
14. 看護
急性心不全において治療のタイミングが遅れることは命に関わります。そのため患者さんの状況の変化を医療者として観察する看護師の眼はとても重要です。また、重症の心不全に対して人工呼吸器管理や補助循環管理が必要な場合は、更にその役割が大きくなります。
- 機械はうまく機能しているか
- 機械のセッティングに問題はないか
- 治療はうまく行っているか
- 患者さんは苦痛を感じていないか
- 鎮静はちょうどよい状況になっているか
- 新たな問題(感染症、褥瘡、出血など)が起こっていないか
これらの項目を毎日確認することになります。変化があった場合は医師などと情報を共有して、現状のアセスメントと治療を追加を検討します。さらに患者さんの知識向上においても、入院中に長く関わる看護師の役割は大きいです。
一方で、慢性心不全でも看護はとても重要です。心不全は小康状態にあるため患者さんが問題に気づきにくい背景がありますが、訪問看護や外来受診時の声掛けによって状態の変化に気づくことも少なくないです。また、看護師が関わることで、心不全患者の日常注意点について再確認できたり、意識を向上させる効果が期待できます。
15. 緩和ケア
心不全には心身の困難が伴うため苦痛を感じることが少なくありません。もちろん心臓が疲れ果てた末期の心不全に対して緩和ケアは必要ですが、急に心臓が悪くなった急性心不全においても緩和ケアは必要です。どんなタイミングの心不全であっても、余計な苦痛を感じる必要はありません。
緩和ケアでは医療者だけでなく患者さんの家族など身近な人にも大切な役割があります。『急性心不全ガイドライン2011』では、患者と周囲の人の関係について次の4つの緩和ケアモデルを示しています。
- 苦しみをキャッチする
- 息切れや動悸などの身体的苦痛
- 動けなくなったことに対する歯がゆさや死への恐怖などの精神的苦痛
- 支えをキャッチする
- 将来の夢
- 支えとなる存在
- 自己決定できる自由
- どのような私たちであれば、患者の支えを強めることができるのかを知る
- 苦しんでいる人にとって、自分の苦しみを分かってくれる人である
- 相手の苦しみをていねいに聴く姿勢(傾聴:反復、沈黙、問いかけなど)
- 支えようとする人の支えを知る
- たとえ力になれなくても逃げないで最期まで関わり続ける関係
- 支えてくれる人は万能ではなく、誰かの支えを必要としていることを認識する
少し難しい話になりましたが、心不全になることで生じる心身の困難を察知して一緒に向き合うことが緩和ケアの根底になります。緩和ケアのプレーヤーは医師や看護師などの医療者だけでなく、患者さんの家族や友人も含まれます。患者さんの背景や歴史を踏まえて周囲のみんながコミュニケーションを図ることで、緩和ケアの第一歩が踏み出されるのです。
また、とても大事なことですが、生活を改善したり内服薬を正しく飲むことで苦痛が緩和されることは多いです。一度、患者さんと家族で生活環境を見直す作業をしてみるようにして下さい。